| Газ | Теплота сгорания, МДж/м3* | Плотность, кг/м3 | Теплота сгорания, МДж/кг |
| Бутан | 124 | 2,588 | 47,9 |
| Метан | 35,9 | 0,714 | 50,2 |
| Пропан | 93,4 | 1,96 | 48,4 |
* – табличное значение согласно справочнику по физике под редакцией Х.Кухлинга
Теплота сгорания пропана и бутана просто покрыта мраком. В сети отсутствуют сертификаты для газовых заправок. Зато на различных сайтах, в зависимости от того, что они пропагандируют (бензин, газ или вообще электричество) приводятся разные значения.
[box type=”shadow” align=”” class=”” width=””]В Википедии для различных языков приведены различные значения!
Так что, может быть они все же они есть, молекулы свободы?))[/box]
Ситуация осложняется тем, в каком состоянии учитывать продукты горения, в частности оксида водорода – воду – в виде пара или в виде воды.
В справочниках так же отсутствуют интересующие нас данные в расчете на килограмм или литр. Но зато есть на кубический метр, при нормальных условиях. Это позволяет вычислить интересующие нас величины.
Итак, в справочники по физике под редакцией Кухлинга 1982 года издания приведены следующие данные:
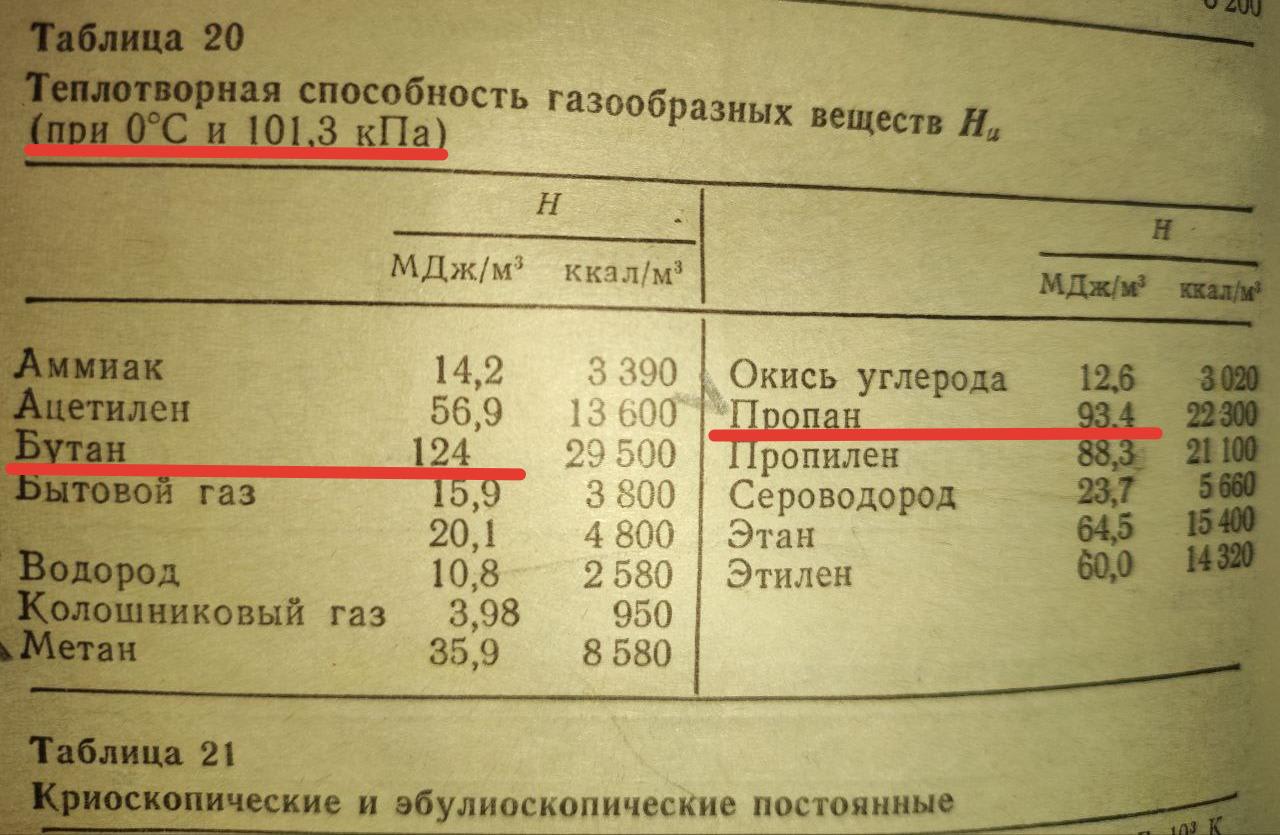
Плотности указанных газов не приведены, но, с учетом того, что:
- универсальная газовая постоянная R равна 8,31 Дж·К⁻¹·моль⁻¹
- 0 °С = 273,15 °K
- молярной массы μ:
- бутана C4H10: 58 грамм/моль
- метана CH4: 16 грамм/моль
- пропана C3H8: 44 грамм/моль
- закона P*V=m/μ * R*T => ρ (грамм/м3)= P/ (R*T) * μ
Получаем:
- P/ (R*T)= 101 300/(8,31*273,15): 44,62 моль/м3
- плотность газообразного:
- бутана: 2,588 кг/м3
- метана: 0,714 кг/м3
- пропана: 1,96 кг/м3
Тогда теплота сгорания составляет:
- бутана: 124 (МДж/м3) /2,558 (кг/м3) = 47,9 МДж/кг
- метана: 35,9 (МДж/м3) /0,714 (кг/м3) = 50,2 МДж/кг
- пропана: 93,4 (МДж/м3) /1,96 (кг/м3) = 48,4 МДж/кг